Полный липопротеиновый спектр крови
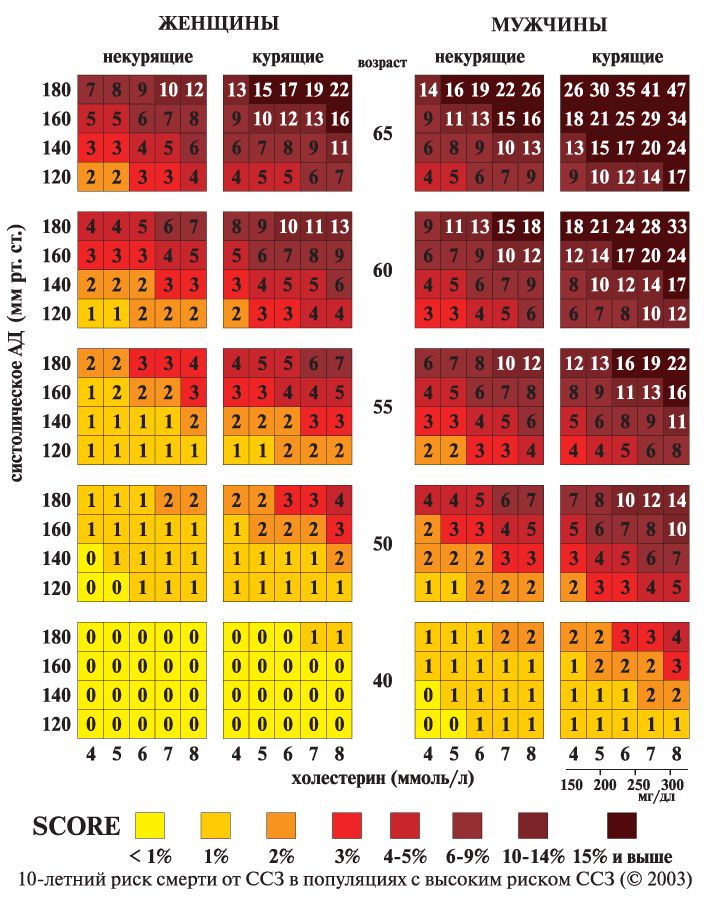
Холестерол содержится в организмах всех животных, но отсутствует в растениях.Он незаменимый компонент всех клеток человека потому, что необходим для образования и восстановления их мембран, клеток и для формирования связей между клетками мозга, что нужно для обучения и памяти, нужен для синтеза гормонов (в частности, половых — эстрогена и тестостерона), а также для образования витамина Д в коже. Треть его мы получаем с пищей, две трети синтезирует печень. Синтез холестерола стимулируют насыщенные жиры, которые содержатся в животной и молочной пище.
Уровень холестерола при рождении ниже 3,0 ммоль/л. С возрастом уровень его в крови увеличивается, появляются половые различия в концентрации.
У мужчин уровень холестерола растет в раннем и среднем возрасте и снижается в старости. У женщин концентрация холестерина с возрастом увеличивается более медленно, вплоть до менопаузы, в дальнейшем может превышать уровень у мужчин.
Это связано с действием половых гормонов. Эстрогены снижают, а андрогены повышают уровень общего холестерина.
Но независимо от всех добрых дел, которые делает холестерол, если в крови его концентрация повышена, это может привести к разным последствиям, в зависимости от того, какой именно холестерол повышен.
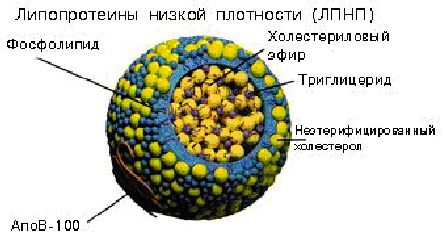 Липопротеины бывают двух основных типов. Первый из них в быту называют «плохим». Правильное его название — холестерол липопротеинов низкой плотности — Х-ЛПНП.
Липопротеины бывают двух основных типов. Первый из них в быту называют «плохим». Правильное его название — холестерол липопротеинов низкой плотности — Х-ЛПНП.
Липопротеины низкой плотности (ЛПНП) при связывании с рецепторами клеток периферических тканей высвобождают холестерол, который в норме используется в процессах синтеза; в результате патологических процессов ЛПНП могут аккумулироваться в тканях, подвергаться модификации и стимулировать образование холестероловых бляшек. Основной белок переносчик Х-ЛПНП — аполипопротеин В (для краткости — АпоВ).
Второй главный игрок метаболизма холестерола — холестерол липопротеинов высокой плотности — Х-ЛПВП. Он «хороший». Именно он обеспечивает «обратный» транспорт: удаление избыточного холестерола из тканей в печень. Х-ЛПВП секретируется печенью и частично кишечником. Основной белок переносчик Х-ЛПВП — аполипопротеин А-1 (для краткости — АпоА1). Попав в печень, Х-ЛПВП расщепляется и содержавшийся в нем холестерол или экскретируется в виде желчных солей или вновь используется для последующего перераспределения в тканях. Иногда Х-ЛПВП называют «мусорщиком» или «дворником» (scavenger) — он очищает от холестерола поверхности клеток и другие липопротеины. Но у Х-ЛПВП есть и другие «хорошие» свойства. В частности, противовоспалительные и антиоксидантные. В общем, «плохой» Х-ЛПНП называют атерогенным — вызывающим атеросклероз, а Х-ЛПВП — антиатерогенным.
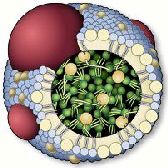 Аполипопротеины — белки, которые расположены на поверхности липопротеинов. Иногда для краткости их называют апопротеинами. Именно апопротеины и определяют, что будет с холестеролом — или он высвободится из «упаковки» и будет поглощен клетками, чтобы потом выполнить свои жизненно важные функции, или наоборот — излишний холестерол, содержащийся в организме, будет удален из тканей и из крови и упакован внутрь липопротеиновой частицы, которая затем унесет его в печень.
Аполипопротеины — белки, которые расположены на поверхности липопротеинов. Иногда для краткости их называют апопротеинами. Именно апопротеины и определяют, что будет с холестеролом — или он высвободится из «упаковки» и будет поглощен клетками, чтобы потом выполнить свои жизненно важные функции, или наоборот — излишний холестерол, содержащийся в организме, будет удален из тканей и из крови и упакован внутрь липопротеиновой частицы, которая затем унесет его в печень.
В марте 2006 года на страницах одного из самых престижных медицинских журналов появился «манифест», подписанный тридцатью специалистами из 10 стран.
Он призывает к установлению новых правил оценки риска сердечно-сосудистых заболеваний (ССЗ). Предлагается заменить общепринятое определение в плазме общего холестерола, Х-ЛПНП и Х-ЛПВП на измерение концентрации АпоВ и АпоА. Ибо риск атеросклероза связан не столько с концентрациями холестерола, сколько с количеством циркулирующих атерогенных частиц и антиатерогенных, которые связываются со стенками сосудов и проникают в артериальные стенки.
Многочисленные исследования убедительно продемонстрировали: именно показатель баланса атерогенных и антиатерогенных частиц АпоВ/АпоА — самый точный индикатор риска ССЗ у лиц с бессимтомными ССЗ и лиц, страдающих диабетом. Более того, отношение АпоВ/АпоА — самый адекватный показатель эффективности терапии, направленной на снижение уровней Х-ЛПНП.
Риск инфаркта миокарда в зависимости от соотношения ApoB/ApoA1
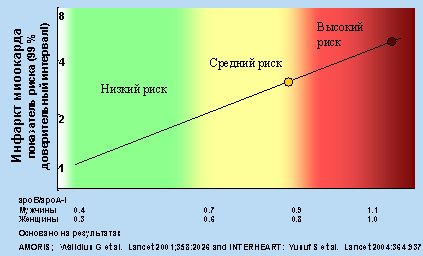
Выявление и детальный анализ нарушения обмена липопротеинов являются основой лабораторной диагностики ранних «доклинических» стадий атеросклеротических поражений. Имеются «рекомендуемые» границы — значения, при которых риск развития атеросклеротических изменений статистически мало вероятен.
В 1988 году экспертными 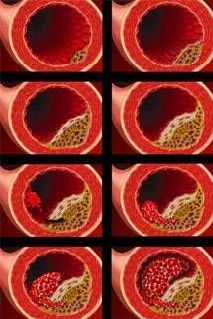 группами национальной образовательной программы по холестеролу в США (National Cholesterol Education Program, NCEP) и Европейского общества по изучению атеросклероза впервые представлена классификация гиперхолестеролемий, отражающая связь уровня общего холестерола и риск ИБС. В 2001 году опубликован новый третий доклад экспертов NCEP, посвященный выявлению, оценке и терапии высокого уровня холестерола у взрослых (Adult Treatment Panel III, ATP III). Основным отличием ATP III является определение риска ИБС по уровню Х-ЛПН, а не общего холестерола сыворотки крови.
группами национальной образовательной программы по холестеролу в США (National Cholesterol Education Program, NCEP) и Европейского общества по изучению атеросклероза впервые представлена классификация гиперхолестеролемий, отражающая связь уровня общего холестерола и риск ИБС. В 2001 году опубликован новый третий доклад экспертов NCEP, посвященный выявлению, оценке и терапии высокого уровня холестерола у взрослых (Adult Treatment Panel III, ATP III). Основным отличием ATP III является определение риска ИБС по уровню Х-ЛПН, а не общего холестерола сыворотки крови.
В зависимости от риска ишемической болезни сердца (ИБС) эксперты предложили выделять несколько уровней (в ммоль/л):
| Желаемый уровень | Выше оптимального | Погранично высокий | Высокий | |
| Общий холестерол | 3.60 - 5.20 | - | 5.21 - 6.21 | > 6.24 |
| Триглицериды |
муж 0.40 - 1.54 жен 0.45 - 1.69 |
1.70 - 2.26 | 2.27 - 5.66 | > 5.67 |
| Холестерол ЛПВП |
муж 0.90 - 1.80 жен 1.16 - 2.10 |
|||
| Холестерол ЛПНП | 2.32 - 3.50 | 2.6 - 3.35 | 3.38 - 4.13 | 4.16 - 4.91 |
| Холестерол ЛПОНП | 0.30 - 0.45 |
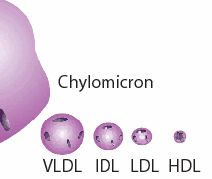 Указывается необходимость всем взрослым людям старше 20 лет каждые пять лет выполнять исследование липидного спектра сыворотки крови.
Указывается необходимость всем взрослым людям старше 20 лет каждые пять лет выполнять исследование липидного спектра сыворотки крови.
Помимо оценки риска развития атеросклероза и его осложнений тесты липидного профиля используют для выявления изменений липидного обмена при ряде других патологических состояний: при заболеваниях печени (изменяется промежуточный обмен липопротеинов), почек (наблюдаются характерные изменения в выведении липопротеинов), эндокринных расстройствах, протекающих с изменениями в регуляции липидного метаболизма (заболевания щитовидной железы, сахарный диабет), ожирении и др.
Показатели липидного обмена во многих случаях поддаются коррекции с помощью диеты (поскольку в значительной степени зависят от количества и состава поступающих с пищей жиров), а также лекарственных средств. Поэтому их целесообразно использовать для контроля проводимого лечения.

Подготовка к исследованию: между последним приемом пищи и взятием крови для исследования должно пройти не менее 12–14 часов. Сок, чай, кофе (тем более с сахаром) — не допускаются. Можно пить воду.






















